エネルギー準位
エネルギー準位
たけ店 さんの書込 (2006/03/17(Fri) 14:14)
はじめまして.浪人決定した1浪生です. この分野は学校で教えてもらえなかったので独学中です.初めて聞くぶんやなのでイメージがしずらい状態です.
質問はというと,「エネルギー順位と電子の軌道半径は関係あるのか」ということなんです.教科書には,「原子にはエネルギー準位ができていて,それらは決まったエネルギーのグループをつくる.これを殻という」とかいてあるんですが,じぶんは,エネルギーのグループ=電子の軌道の半径,とかなんかわけのわからない解釈をしてしまい,かなり混乱しています・・・・.うまく説明できませんが・・.
また,化学では,電子と陽子は電荷を帯びているため,たとえば塩化イオンよりアルゴンのほうが陽子の数が多いため強く引き合うから,塩化イオンより半径がちいさくなるような風に習っているためさらに混乱しています・・・.
話は長くなってしまいましたが,なにとぞよろしくお願いします.
Re: エネルギー準位
渡邉 さんのレス (2006/03/17(Fri) 14:28)
どうもはじめましてたけ店さん.
「エネルギー準位と電子の軌道半径は関係あるのか」 を知る目的は何ですか?
僕は,化学結合のメカニズムに興味があるのかな?と直感しました.ほんとうのところは,どうなのでしょうか? それが分かれば,僕はたけ店さんと協力できるかもしれません.
Re: エネルギー準位
篠原 さんのレス (2006/03/17(Fri) 14:56)
たけ店さん,こんにちは. 篠原です.
まず,電子は,原子核の周りを電子雲として,確率的に分布しているのは,良いでしょうか? このため,例えば「半径1Åの円軌道を描いている」というような表現はできず,電子の軌道の半径を議論するときには,「その電子がどの程度の広がりを持っているか」という議論になるかと思います. (この部分が難しくてわからなければ,お気軽に再度質問してください.)
これを踏まえた上で,エネルギー準位と軌道半径のことを述べますと, 定性的には,エネルギーが低い準位ほど,軌道半径が小さいということはできます. これは,プラスの電荷を持った陽子とマイナスの電荷を持った電子のクーロンポテンシャルが,その間隔が短いほど小さくなるためです.
また,量子力学をきちんと(大学で)習うとわかるのですが,電子の軌道を決定するのに,主量子数n,方位量子数l,磁気量子数m,スピン量子数s,という4つの量子数を考えることができます. (n,l,m,s)の組が決まると,対応した軌道をひとつだけ決めることができ,それに対応したエネルギーも決まります. 実は,n=1の場合をK殻,n=2の場合をL殻 と化学では呼んでいます. そして,主量子数が決まると,「およそのエネルギーと半径」が決まります. この,主量子数の同じグループのことを, 化学では殻と呼んでいるわけです.
ただし,ここで「およそのエネルギー」といったのは,エネルギーは主量子数だけで決まるわけでなく,他の量子数にも依存するからです. このことが原因で,周期律表のあの変な形ができるわけですが,詳しくは大学の量子力学で・・・.
追加 ゆっくり書いている間に 渡邉さんと入れ違いになったようですね. 渡邉さん,こんにちは&すみません. たけ店さん,私の書き込みで,逆に混乱するようでしたら,無視してください.
Re: エネルギー準位
たけ店 さんのレス (2006/03/18(Sat) 01:20)
こんばんは.ご返答ありがとうございます.
知りたい目的は,化学結合(結晶)ででてくるエネルギーバンドについてなんですけれども,実は疑問が多少あったため,教科書に書いてある順番にひとつずつ疑問を消化していこうとおもいました. また,渡邉さんのおっしゃるとおりで化学結合についてのメカニズムについては大いに興味があります.欲張りすぎて,またわからないことが多いので,質問がしつこくなるかもしれませんが大目に見てください^^;
篠原さんのコメントについてですが,「電子は,原子核の周りを電子雲として,確率的に分布している」というのはどういうことでしょうか.本当にここの分野については基礎(言葉)からしてうまくイメージできない状態なんで,どういうものか(具体例とか)があるとたすかりますm(__)mこの文でしたら電子雲や,確率的に存在する,といった意味がわかりません^^;
余談ですが,実はこの分野は来年の入試の範囲には入っていないのです.しかし個人的にかなり興味があるので勉強しています.何度教科書をよんでもわかりませんでした.ですから,混乱してもなにしてでも理解したいのです.執着心は人一倍ありますうざいかもしれないけど・・・.篠原さんのおっしゃられていることにかなり興味があるんです.いわれると,理解できないうちは気になって夜も眠れないです.大げさかもしれませんが(笑)無視なんかできるわけないです.馬鹿ですけどプライドだけはでっかいでんす(笑)
話は戻りますが,化学結合では原子の価電子が関係しているんですよね.となると,エネルギーが低いほど軌道半径が小さい=(イコール)K殻がいちばんエネルギーが小さい=熱などのエネルギーを加えた場合最初に飛び出す電子はK殻にあるでんし,ではないんでしょうか.
私のコメントに多少の失態があると思われるかもしれませんが,よろしくお願いいたします
Re: エネルギー準位
篠原 さんのレス (2006/03/18(Sat) 01:56)
こんばんは. 篠原です.
>「電子は,原子核の周りを電子雲として,確率的に分布している」というのはどういうことでしょうか.
電子は,原子核の周りを,円を描いて回っている太陽と地球のようなモデルではなく,下のサイトにあるような,形の体積の中に,確率的に分布しているということです.
「確率的に」というのは,これらの体積の中の「どこかに」電子がいる,ということです. 電子がいる場所は,正確に決めることができず,「あっちにいるかもしれないし,こっちにいるかもしれない」といった状況です. 古典的には,電子は粒子として,ある一点にいると考えるのですが,量子力学では,上のサイトの体積のように,ある広がりを持って存在しているため,これを「電子の雲」のように考える,すなわちこれを「電子雲」と呼んでいるわけです. きっと,意味がわからないでしょうが,私も本質的に理解できているわけではありません. これが,量子力学の教えるところなのです.
>しかし個人的にかなり興味があるので勉強しています.
いいですね! 私は,ぜひともあなたを応援したいです. でも,あまり難しい分野まで,いきなり手を出すと,混乱するだけですよ. 基本的な分野をきちんと理解しないと,その先の面白いところを理解することはできません. 基本的な分野も,きちんと勉強してくださいね :)
また,「エネルギーが小さい」というのは,真空中に静止している電子に比べて,原子核に束縛されている電子のほうが安定である,ということです. 真空中に静止している電子のエネルギーを 0eV とすると, (このエネルギー準位を真空準位と呼びます.eV は,エネルギーの単位です.) それに比べて,束縛されている電子は,例えば -10eV などの値になります. 頭にマイナスがついているため,真空準位より低いエネルギーになりますが,原子からこの電子を取り出すには, 10eV のエネルギーが必要になります. つまり,エネルギーの小さい準位ほど,取り出すのにエネルギーがたくさん要るため,熱などによって飛び出してくる電子は,一番エネルギーの高い電子になります. K殻は,一番取り出しにくい電子の軌道ということになりますね.
バンドに関して知りたいと言う事ですが,当サイトにもバンドに関する記事があります. 「固体物理学」カテゴリ内
導体・絶縁体・半導体 (篠原著) バンドの形成 (NOBU著)
これらの記事が参考になるかと思います. ぜひ,ご一読ください :)
Re: エネルギー準位
CB さんのレス (2006/03/18(Sat) 02:12)
初めまして たけ店さん.
高校物理はどの程度の内容までやるのか記憶があやふやですが,答えられる範囲でお答えします.
>エネルギーのグループ(殻のこと?)=電子の軌道の半径 原子における電子のエネルギー準位とは中心力場におけるポテンシャルが起源なので,模型的に考えて"中心に近いほどエネルギー準位は小"と考えて全く問題無いと思います.
>電子は,原子核の周りを電子雲として,確率的に分布している これは「量子力学での解釈で電子を考える」と,ということです. 量子力学以前は,電子は太陽と地球のような軌道で運動していると考えられていましたがそれでは説明がつかないことが出てきました.それで,ボーアとかプランクとかシュレーディンガーとかディラックとか・・・色々と大先生方ですったもんだして「電子のような微小な粒子は確率でしか表せない.つまり,この場所にはこのくらいの確率で存在しているということしかいえない」って感じの結論に至りました.それを"確率的に分布している"とか電子雲というふうに表現したりします.
>エネルギーが低いほど軌道半径が小さい・・・ エネルギー準位という言葉を誤解しているようですね.この場合のエネルギー準位とは自由電子(核に束縛されていない状態)を基準にしています(エネルギー=0).エネルギー0で原子核の束縛から逃れられる状態になるということです. 核(中心)に近づくにつれて負の値になります.つまりK殻(最も核に近い)は負の値が大きい(値は最小)ということです.
「エネルギー準位が低い」とは「それだけ多くのエネルギーを与えないと外に出られない」ということです.つまり一番強く束縛されているのはK殻の電子だと言うことです.
夜も深い時間だらだらと考えていたら篠原さんとかぶってしまいました... こんばんわ >篠原さん 上の説明の方がわかりやすいと思います.眠い頭で書いたものなので混乱するようでしたらサラっと流してください >たけ店さん
Re: エネルギー準位
たけ店 さんのレス (2006/03/18(Sat) 02:22)
なるほど!めっちゃわかりやすいです.確かにそうですね,電子はすべてマイナスの電荷だから,真空をゼロとしたら,エネルギーが小さくなればなるほど大きなエネルギーが必要になりますね.電子は粒子でもあり波でもあるから,場所がわからないけど,確率的に存在するというのは聞いたことがありました.このことだったとはしりませんでしたが.
さらに二つの質問ですが,原子が安定するのはどうして希ガス元素なんでしょうか. また,エネルギー準位と殻が関係しているとしたら,どうしてその殻によって入る数は決まっているのでしょうか.自分ではエネルギーさえ満たしていればK殻にはいくらでも電子が入ることができると思うんですが. よろしくお願いします
エネルギーバンドについては,もうちょっとここの疑問を納得してからききます^^;頭がこんがらがるので.また,基本的といいますか,一通り受験で勉強したので,電気,力学,波動は大丈夫だと思います.高校の範囲でですけど・・・.
Re: エネルギー準位
渡邉 さんのレス (2006/03/18(Sat) 11:36)
とても良い流れになってきたと思います.これが,僕にとっては「マンガの問題」につながるわけです.この今の「構造」を研究して,どうにか「きれい」な部分を見出したいところです.そのためには,僕が見ていない間の変化を,時間をかけて追って,「消化」する必要があると思っています.
Re: エネルギー準位
CB さんのレス (2006/03/18(Sat) 12:23)
>どうしてその殻によって入る数は決まっているのでしょうか この疑問こそ まさに量子力学です!!
教科書的な答えは「パウリの排他律があるから」です. その個数はシュレーディンガー方程式(量子力学版ニュートン運動方程式のようなモノ)によって導出できます.
これは完全に大学レベルの内容ですね...
Re: エネルギー準位
篠原 さんのレス (2006/03/18(Sat) 13:13)
篠原です
CBさん,渡邉さん,こんにちは.
すべての電子がK殻に入れないのは,CBさんがおっしゃるように,「パウリの排他律」が原因です. 一度,ご自分でパウリの排他律について,調べてみてください. きっと何かわかるでしょう.
また,以下のサイトが参考になるかと思います.
この中の,「Science Trek」内の,「The Periodic Table」が大変良い参考になるのではないでしょうか. この中から,どうして希ガスが安定なのか,気がつくことができるかもしれませんよ :)
今回は,私からはヒントを差し上げるだけにします. 自分で調べていると,他にもいろいろなことに気がつけるかもしれませんよ. がんばってください!
Re: エネルギー準位
たけ店 さんのレス (2006/03/18(Sat) 16:48)
忙しい中,ご返答に大変感謝しています.ありがとうございます.
ざっと出はありますが,パウリの排他律について調べてみました.とてもわかりやすく書いてくれているのかもしれませんが,大学でつかうような言葉が次々とでてきて一個一個調べていると,何を理解しようとしてるのがだんだんわからなくなってしまいました・・・.混乱とまではいきませんが.でも自分なりの解釈をしてみたんで,この場を借りて聞いてください.
パウリの排他律というのは「同じ電子軌道の中に,同じ量子状態の電子が入ることはできないということ」ですよね.これに対して私は,量子状態には四種類あって,同じ量子状態でなければ同じ殻に入ることができるということと解釈いたしました.となるとK殻にはやはり,量子状態さへかぶらなければ,二個以上の電子が入ることが可能ではないのでしょうか.もしも,大変難しい知識が必要であれば,ここはこうである!という定義としてご教授いただけるとうれしいです.私もそれはそうなんだ!として納得しますんで.
またせっかく化学の安定について,よいサイトを教えていただいたにもかかわらず文章を読んでいるうちにわけがわからなくなりました.単語が簡単でもいろいろな意味を含んでいたり,どれが正しいのかわからなくなって挫折してしまいました.自分でも検索してみたんですがうまく見つからず,大変無礼ではありますが,簡単な説明をお願いできないでしょうか.
Re: エネルギー準位
CB さんのレス (2006/03/18(Sat) 18:48)
>量子状態さへかぶらなければ,二個以上の電子が入ることが可能ではないのでしょうか その量子状態に上限があるということです.K殻の量子状態の上限が2つ,L殻が8つ,となるということです. それじゃこの数字はどうやって出てくるのかということですが・・・
先に出てきたシュレーディンガー方程式を解くとエネルギー準位が算出できます.その結果はこのようになります.
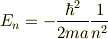
注目は後半の分数です(  は自然数).
原子の周りを回る電子のエネルギーはとびとびの値(自然数)しか取れないよということです.この
は自然数).
原子の周りを回る電子のエネルギーはとびとびの値(自然数)しか取れないよということです.この  を主量子数(エネルギー値を決めている張本人)といいます.
そして
を主量子数(エネルギー値を決めている張本人)といいます.
そして 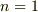 をK殻,
をK殻, 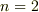 をL殻,と順に名前つけたということです.
をL殻,と順に名前つけたということです.
さらに話は複雑になるのですが,この主量子数のほかに方位量子数,磁気量子数というのがあり主量子数  と方位量子数
と方位量子数 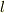 ,磁気量子数
,磁気量子数 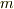 の関係は次のようになります.
の関係は次のようになります.
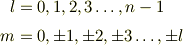
さらにスピン状態がupspinとdownspinと2つの状態があります.
以上をまとめると電子の量子状態はつぎのようになります.
[K殻] n=1 l=0 m=0 でスピン状態が2つで状態が2つ
[L殻] n=2 l=0 m=0 l=1 m=-1 m=0 m=1 でスピンがそれぞれ2つあるので状態は8つ
という感じです. 大学1年でもまだ習わない内容だと思います.かなり天下り的な説明ですが理解の一助になれば...
Re: エネルギー準位
たけ店 さんのレス (2006/03/19(Sun) 00:03)
わかりやすい説明大変ありがとうございます.
なるほど,エネルギーがnのとき主量子数l=n−1の数を取り,磁気量子数m=±lの数を取る,またスピンに二種類存在するため,組み合わせで殻に入る数が決まるというわけですね. 私は大学一年でも学ばない分野に足を入れてるわけですか・・・.あまり深入りしないよう気をつけます・・・.
ほんとにありがとうございました.また,エネルギーバンドについての質問なんですが聞いていただけないでしょうか.
Re: エネルギー準位
篠原 さんのレス (2006/03/19(Sun) 02:07)
>また,エネルギーバンドについての質問なんですが聞いていただけないでしょうか.
質問があるなら,質問すればいいですよ :) ただ,どの辺に疑問を持っているのか,どの程度調べて,どのくらいまではわかったのか,などを明記した上で質問すると,より良い返答が返ってくるでしょう. また,今までの続きではなく,質問内容が少し変わるようでしたら,新しくスレッドを立てて質問したらよいでしょう.
「入試には関係ないけど興味があるから勉強しています」という姿勢,とても良いことだと思います. 高校での勉強は,単なる大学入試のための勉強ではなく,大学入学以降の研究のための勉強と私は考えているからです. 私のわかる範囲内で,質問にはお答えしたいです. ですので,がんばってください!